Les transformations chimiques

Qu’est-ce qu’une transformation chimique ?
Une transformation chimique a lieu lorsque une substance (de la matière) se transforme en une autre substance (différente de celle de départ).
La plupart du temps cette transformation est facile à détecter car la substance de départ et la substance à l’arrivée ne se ressemblent pas (couleurs différentes, odeurs différentes, pas le même état physique…).
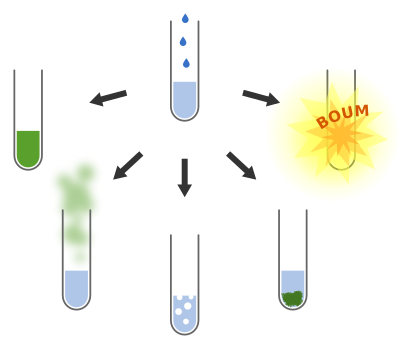
En pratique, on constate donc généralement qu’une transformation chimique a eu lieu si on observe :
- un changement de couleur ;
- un changement d’odeur ;
- l’apparition d’un dégagement gazeux ;
- l’apparition d’un solide (qu’on appelle un précipité) ;
- une flamme ou une explosion !
Autres transformations
Il existe d’autres transformations qui ne sont pas des transformations chimiques comme par exemple les transformations physiques au cours desquelles les substances de départ et les substances d’arrivée sont les mêmes mais sous des formes différentes. Plusieurs cas sont possibles :
- un changement d’état physique (voir le cours sur les états de la matière) ;
- un mélange de plusieurs substances (voir le cours sur les mélanges) ;
- une déformation…
Attention : certaines transformations physiques peuvent ressembler à des transformations chimiques (par exemple deux substances colorées peuvent donner un mélange d’une autre couleur ; il y a un changement de couleur mais sans transformation chimique).
Réactifs et produits
Lors d’une transformation chimique, les substances de départ qui disparaissent sont appelées des réactifs et les substances qui apparaissent à l’arrivée sont appelée des produits.
Par exemple lors de la photosynthèse, les plantes transforment l’eau du sol et le dioxyde de carbone de l’air en dioxygène et en glucose. Il s’agit d’une transformation chimique car les substances de départ (l’eau et le dioxyde de carbone) ne sont pas les mêmes que celle d’arrivée (le dioxygène et le glucose). Les réactifs sont l’eau et le dioxyde de carbone et les produits sont le dioxygène et le glucose.
Les substances présentes lors de la transformation mais qui ne réagissent pas sont appelées des substances spectatrices.
Bilan d’une transformation
Pour simplifier l’écriture de ce qui se passe lors d’une transformation chimique, les scientifiques notent ce qu’on appelle le bilan de la transformation.
Le bilan d’une transformation chimique ressemble un peu à une équation mathématique : on écrit tous les noms des réactifs séparés par des signes + à gauche d’une flèche → ; puis à droite de la flèche, on écrit tous les noms des produits séparés par des +.
réactif 1 + réactif 2 + … → produit 1 + produit 2 + …
Pour la photosynthèse de l’exemple précédent, le bilan s’écrit :
eau + dioxyde de carbone → dioxygène + glucose
Conservation de la masse
À la fin du XVIIe siècle, le chimiste français Antoine Lavoisier réalise des transformations chimiques et détermine avec une très grande précision la masse de tous les réactifs et de tous les produits (y compris ceux sous forme gazeuse). Il remarque alors que la masse des réactifs est toujours égale à celle des produits.
Sa conclusion est restée célèbre : « Rien ne se perd, rien ne se crée, tout se transforme » !
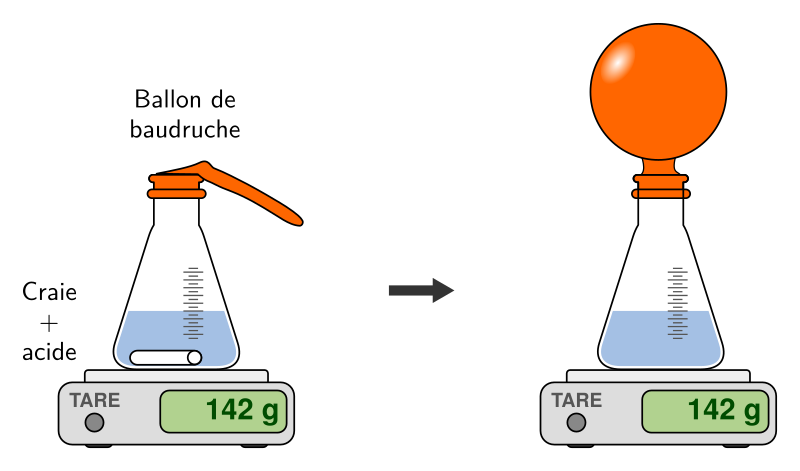
Lors d’une transformation chimique, la masse se conserve.
Par exemple, lorsqu’on place une craie dans de l’acide, celle-ci disparaît et un gaz se forme. Si on mesure la masse de la craie et de l’acide au départ, et qu’on la compare à la masse du mélange obtenu et du gaz libéré à la fin, on obtient la même valeur :